Rage
Rabies lyssavirus — famille des Rhabdoviridae, genre Lyssavirus
Encéphalite virale mortelle à ~100 % une fois symptomatique, mais entièrement évitable par la prophylaxie. La vaccination pré-expositionnelle (PrEP) élimine le besoin d'immunoglobulines antirabiques — souvent introuvables à l'étranger. La PEP doit être initiée sans délai après toute exposition suspecte.
Épidémiologie
Données mondiales
- Environ 59 000 décès/an (OMS), probablement sous-estimé ; 95 % des cas en Asie et en Afrique[1,2]
- ~40 % des victimes sont des enfants de moins de 15 ans[1]
- 99 % des cas humains sont transmis par des chiens domestiques[1]
- Objectif mondial « Zero by 30 » : élimination des décès humains par rage canine d'ici 2030 (OMS/OIE/FAO)[1]
Situation en Suisse
- Aucun cas humain autochtone depuis 1977 ; rage terrestre éliminée chez le renard depuis 1999[3,4]
- Seul réservoir persistant : chauves-souris (European Bat Lyssavirus 1 et 2)[3]
- Chaque année : plusieurs dizaines de consultations pour exposition potentielle à la rage chez les voyageurs (morsure/griffure à l'étranger)[3]
- Risque résiduel : morsure de chauve-souris en Suisse ; importation illégale de chiens/chats depuis pays endémiques[3,4]
Risque pour les voyageurs
- Incidence d'une blessure à risque : environ 0,4 % des voyageurs par mois de séjour en zone endémique[5]
- Données GeoSentinel (1997–2012) : 2 697 voyageurs ayant nécessité une PEP ; 70 % des expositions en Asie (surtout Asie du Sud-Est) ; durée médiane du voyage de seulement 15 jours[5,6]
- Animaux impliqués chez les voyageurs : chiens (60–80 %), singes (5–15 %), chats (10–15 %)[5,6]
- Seulement 2–3 % des voyageurs sont vaccinés contre la rage avant le départ[6]
Répartition géographique
La rage est présente sur tous les continents sauf l'Antarctique. Les zones de risque le plus élevé pour les voyageurs sont l'Asie du Sud et du Sud-Est (Inde, Bangladesh, Thaïlande, Cambodge, Vietnam, Indonésie), l'Afrique sub-saharienne et dans une moindre mesure l'Amérique latine. L'Inde concentre à elle seule environ un tiers des décès mondiaux.
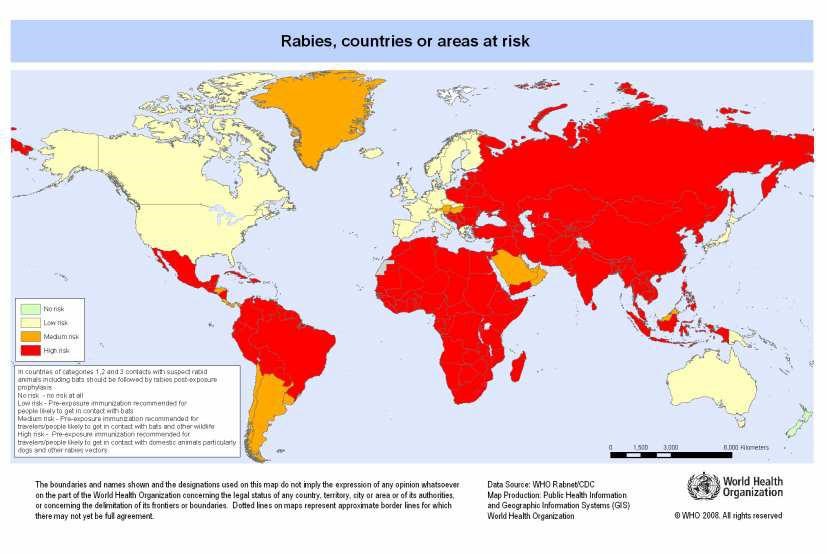
Zones sans rage terrestre
Europe occidentale (y compris la Suisse depuis 1999), Japon, Australie, Nouvelle-Zélande, Hawaï, de nombreuses îles du Pacifique et des Caraïbes. Attention : des lyssavirus de chauves-souris circulent dans plusieurs de ces pays, y compris en Europe.[3,8]
Transmission
- Morsure d'un animal enragé (voie principale) : inoculation du virus par la salive dans le tissu sous-cutané/musculaire[1]
- Griffure contaminée par la salive
- Léchage d'une plaie ouverte ou d'une muqueuse (yeux, nez, bouche) — catégorie III si muqueuse[1,7]
- Contact avec chauve-souris : morsure souvent imperceptible (dents très fines) — considéré comme catégorie III par défaut[1,7]
- Transmission interhumaine : extrêmement rare, documentée uniquement lors de transplantations d'organes[1]
Classification OMS des expositions
| Catégorie | Type de contact | PEP requise |
|---|---|---|
| I | Toucher/nourrir l'animal, léchage sur peau intacte | Non (pas d'exposition réelle) |
| II | Mordillage sur peau découverte, griffure/abrasion mineure sans saignement | Vaccination immédiate |
| III | Morsure(s) transdermique(s), griffure(s) avec saignement, léchage sur muqueuse ou peau lésée, tout contact avec chauve-souris | Vaccination immédiate + immunoglobulines antirabiques (RIG) |
Adapté de : OMS, Position paper 2018[1] et recommandations OFSP 2021[3,7]
Présentation clinique
Incubation
- Habituellement 20–90 jours, mais peut varier de quelques jours à > 1 an (cas documentés jusqu'à 6–7 ans)[1,8]
- Facteurs raccourcissant l'incubation : morsure à la tête/cou/mains (zones très innervées), morsures multiples/profondes, inoculum viral élevé
- Implication clinique : la PEP doit être initiée même des mois après une morsure non traitée — il n'est jamais trop tard[7]
Phase prodromique (2–10 jours)
- Céphalées, fièvre, malaise général, myalgies
- Paresthésies/douleur/prurit au site de la morsure — signe quasi-pathognomonique, présent dans ~50–80 % des cas[8]
- Nausées, vomissements, pharyngalgie
Rage furieuse (encéphalitique) — 80 % des cas
- Agitation, hyperexcitabilité, hallucinations
- Hydrophobie : spasmes du pharynx/larynx à la vue ou au bruit de l'eau — signe classique
- Aérophobie : spasmes provoqués par un courant d'air
- Hypersalivation, convulsions
- Épisodes de lucidité entre les crises
- Évolution vers coma et décès en 2–10 jours
Rage paralytique — 20 % des cas
- Paralysie flasque ascendante (début au membre mordu)
- Confusion diagnostique fréquente avec le syndrome de Guillain-Barré[8]
- Évolution plus lente (jusqu'à 30 jours) vers paralysie respiratoire et décès
| Caractéristique | Rage furieuse (80 %) | Rage paralytique (20 %) |
|---|---|---|
| Présentation dominante | Agitation, hydrophobie, aérophobie | Paralysie flasque ascendante |
| Conscience | Épisodes de lucidité alternant avec agitation | Relativement préservée initialement |
| Diagnostic différentiel principal | Encéphalite virale, tétanos | Guillain-Barré, poliomyélite |
| Durée jusqu'au décès | 2–10 jours | Jusqu'à 30 jours |
⚠ Létalité ~100 %
Une fois les symptômes déclarés, l'évolution est virtuellement toujours fatale. À ce jour, < 30 cas de survie documentés dans la littérature mondiale, presque tous avec séquelles neurologiques sévères.[9] Il n'existe aucun traitement curatif — le protocole de Milwaukee est considéré comme un échec (Jackson AC, CID 2025).[9,10]
Diagnostic
Ante mortem
- Clinique + anamnèse d'exposition : pilier du diagnostic
- RT-PCR sur salive, biopsie cutanée (nuque, follicules pileux), LCR — sensibilité variable, répétition recommandée[8]
- Immunofluorescence directe (DFA) sur biopsie cutanée (nuque)
- Sérologie : anticorps neutralisants dans le sérum et le LCR — positive uniquement chez les patients non vaccinés (apparition tardive)
- IRM cérébrale : anomalies non spécifiques (hippocampe, tronc cérébral)[8]
Post mortem
- DFA sur tissu cérébral (gold standard)
- RT-PCR sur tissu cérébral
Diagnostic différentiel
| Diagnostic | Éléments distinctifs |
|---|---|
| Encéphalite virale (herpès, arboviroses) | Pas d'hydrophobie/aérophobie ; IRM et PCR LCR orientent |
| Syndrome de Guillain-Barré | Mimique de la rage paralytique ; dissociation albumino-cytologique au LCR |
| Poliomyélite | Paralysie asymétrique, pas de troubles sensitifs |
| Tétanos | Trismus, opisthotonos, pas de troubles de conscience |
| Encéphalite à virus West Nile | Paralysie flasque aiguë ; sérologie/PCR |
| Intoxication anticholinergique | Mydriase, tachycardie, rétention urinaire, contexte toxicologique |
Traitement
Aucun traitement curatif n'est disponible une fois les symptômes apparus. Le protocole de Milwaukee (coma thérapeutique induit + antiviraux), développé en 2004, a été formellement abandonné en 2025 par son propre promoteur (Jackson AC, CID 2025).[9] Le taux de survie était < 5–10 %, avec séquelles neurologiques sévères chez la quasi-totalité des survivants.[9,10]
⚠ Message clé
La prévention (PrEP + PEP) est la seule stratégie efficace. Il n'existe aucun traitement curatif de la rage symptomatique.
PrEP — Prophylaxie pré-expositionnelle
Indications (OFSP/CFV 2021, Plan de vaccination suisse 2025)
- Professionnels exposés : vétérinaires, étudiants vétérinaires, laborantins rage, chiroptérologues, taxidermistes[3,4,11]
- Voyageurs se rendant dans des pays où la rage est très répandue :
- Séjour > 1 mois en Asie du Sud/Sud-Est ou en Afrique sub-saharienne
- Séjour > 6 mois en Amérique latine
- Activités à risque : randonnée, tour à vélo, spéléologie, contact avec animaux
- Zones à accès limité aux soins médicaux (RIG souvent indisponible)
Schéma PrEP (OMS 2018 / OFSP 2021)
| Voie | Schéma | Rappel |
|---|---|---|
| IM | 2 doses à J0 et J7–J28 (intervalle minimal 7 jours) | 3e dose après 12 mois si nouveau voyage à risque ou exposition continue |
| ID (0,1 mL) | 2 doses à J0 et J7 (schéma dose-sparing OMS) | Idem |
- Pas de sérologie de contrôle nécessaire en routine après PrEP chez les immunocompétents[1,11]
- 2 doses ID J0–J7 : non-inférieur au schéma 3 doses classique chez l'adulte immunocompétent[12]
- Réponse anamnestique documentée jusqu'à 3 ans après une PrEP 2 doses, avec rappel efficace[12,13]
- Chez les immunodéprimés : schéma 2 doses valide mais sérologie de contrôle recommandée[13]
Avantages majeurs de la PrEP pour les voyageurs
- Élimine le besoin d'immunoglobulines antirabiques (RIG) en cas d'exposition — RIG souvent introuvable hors des grandes villes[14,15]
- Simplifie la PEP : seulement 2 doses de rappel (J0, J3) au lieu de 4 doses + RIG
- Allonge le délai acceptable pour initier la PEP (marge de sécurité accrue)
- Coût global : la PrEP est souvent moins coûteuse qu'une PEP complète avec rapatriement sanitaire[15]
PEP — Prophylaxie post-expositionnelle
1. Soins immédiats de la plaie
⚠ Geste salvateur n°1
Lavage immédiat à l'eau courante + savon pendant 15 minutes minimum, puis désinfection (povidone-iodée ou alcool 70 %). Ce geste seul peut réduire le risque de rage de ~90 %.[7]
- Ne pas suturer la plaie (ou si indispensable : sutures lâches, minimales, après infiltration de RIG)[1,7]
- Prophylaxie antitétanique selon statut vaccinal
- Antibiothérapie si plaie profonde/souillée
2. Schéma PEP chez les patients NON vaccinés
Recommandations OFSP 2021 / OMS 2018[3,4,7,11]
| Catégorie | Vaccin antirabique | Immunoglobulines (RIG) |
|---|---|---|
| II | IM : J0, J3, J7, J14 (4 doses) ou ID (2 sites) : J0, J3, J7 |
Non |
| III | IM : J0, J3, J7, J14 (4 doses) ou ID (2 sites) : J0, J3, J7 |
Oui — Bérirab (HRIG) 20 UI/kg Infiltrer un maximum dans et autour de la plaie NB : il n'est plus recommandé d'administrer le volume restant en IM[4] RIG au J0, au plus tard J7 après la 1re dose de vaccin |
Sérologie à J21 avec injections supplémentaires en fonction du résultat.[4]
3. Schéma PEP chez les patients PRÉALABLEMENT vaccinés (≥ 2 doses PrEP)
| Vaccin | RIG | Sérologie |
|---|---|---|
| IM : J0 et J3 (2 doses de rappel) | Non — quel que soit le délai depuis la vaccination | J14, injections supplémentaires selon résultat[4,11] |
4. Points critiques de la PEP
- Pas de contre-indication à la PEP : grossesse, allaitement, immunosuppression, nourrisson — la PEP doit toujours être administrée[1,7]
- Il n'est jamais trop tard pour débuter la PEP, même si l'exposition remonte à des semaines ou des mois[7]
- Délai idéal : dans les 24 heures suivant l'exposition (recommandation OMS)[1]
- Si l'animal peut être observé pendant 10 jours (chien, chat, furet) et reste sain : la PEP peut être interrompue[7]
- Si l'animal est une chauve-souris : PEP toujours indiquée (catégorie III par défaut), même en l'absence de morsure visible[3,7]
5. Problématique de la disponibilité de la PEP à l'étranger
⚠ Données récentes : de Feij et al., J Travel Med 2025
- Étude sur 1 410 voyageurs néerlandais (2019–2024) avec blessure animale à l'étranger[14]
- 59,4 % ont subi un retard dans l'initiation de la PEP
- Facteur principal de retard : besoin de RIG — OR 6,46 (IC 95 % : 4,26–9,79)
- 65 voyageurs (7,8 %) ont dû être rapatriés faute de RIG disponible sur place
- Retard le plus élevé : Amérique centrale et du Sud (médiane 4,5 jours pour les RIG)
6. Anticorps monoclonaux — alternatives aux RIG
- Rabishield (Serum Institute of India) : premier anticorps monoclonal antirabique approuvé (Inde, 2016) ; étude post-homologation (Lancet 2025, n > 4 000) : non-inférieur à l'ERIG, mieux toléré ; dose fixe de 3,33 UI/kg[17]
- Docaravimab + miromavimab (cocktail mAb) : profil de sécurité favorable (Nature 2025)[18]
- CRM25 : cocktail mAb humain avec neutralisation large incluant les lyssavirus non-RABV[19]
- Ces anticorps monoclonaux pourraient résoudre la pénurie mondiale de RIG à moyen terme, mais ne sont pas encore disponibles en Suisse
Prévention
- Éviter tout contact avec des animaux en zone endémique (chiens errants, singes dans les temples, chats, chauves-souris)
- PrEP avant le voyage : 2 doses IM J0–J7 (schéma court possible juste avant le départ)[4,11,20]
- Éduquer les voyageurs : en cas de morsure, laver immédiatement 15 min à l'eau et au savon puis consulter dans les 24 h
- Conserver le carnet de vaccination en voyage
- La PrEP ne dispense pas de la PEP après une exposition (mais la simplifie considérablement)
Pièges & perles cliniques
« La Suisse est exempte de rage, pas besoin de PEP »
FAUX pour les voyageurs exposés à l'étranger : la PEP doit être initiée/complétée au retour si non faite sur place. FAUX pour les contacts avec chauves-souris en Suisse : EBLV-1/2 circule chez les chiroptères européens.[3]
« L'animal avait l'air sain, pas de risque »
FAUX : un animal peut excréter le virus 5–10 jours AVANT l'apparition des symptômes. En zone endémique, toute morsure de chien/chat non vacciné = exposition potentielle.[1]
« La morsure date de 3 mois, c'est trop tard pour la PEP »
FAUX : il n'est JAMAIS trop tard pour initier la PEP — l'incubation peut durer > 1 an.[7]
« Le voyageur est vacciné, pas besoin de consulter après une morsure »
FAUX : la PrEP ne dispense PAS de la PEP (2 doses de rappel nécessaires après exposition).[4,11]
« Les RIG seront disponibles sur place en cas de besoin »
FAUX : 59 % des voyageurs subissent un retard de PEP à l'étranger ; 7,8 % sont rapatriés faute de RIG. En Inde, les RIG ne sont disponibles que dans 20,3 % des établissements publics. C'est l'argument principal pour recommander la PrEP.[14,16]
Perles
Lavage de la plaie 15 min
Ce geste simple à l'eau et au savon est le plus important de toute la prise en charge initiale. Il peut réduire le risque de rage de ~90 % même sans PEP.[7]
PrEP 2 doses en 1 semaine
Un des meilleurs investissements en médecine du voyage : élimine le besoin de RIG et de rapatriement urgent. Schéma court J0–J7 possible même juste avant le départ.[12,20]
Chauve-souris = catégorie III
Toute morsure de chauve-souris (y compris en Suisse) nécessite une PEP complète, même si aucune lésion n'est visible. Les morsures de chauves-souris sont souvent imperceptibles.[3,7]
Conduite pratique pour le médecin de premier recours
Scénario 1 : Consultation pré-voyage
- Évaluer le risque d'exposition : destination (Asie du Sud/Sud-Est, Afrique = risque élevé), durée, activités prévues, accès aux soins sur place
- Recommander la PrEP largement : 2 doses IM J0 et J7 (schéma court possible juste avant le départ) — la PrEP élimine le besoin de RIG, souvent introuvable[14,15]
- Éduquer le voyageur :
- Éviter de toucher/nourrir les animaux (chiens errants, singes dans les temples)
- En cas de morsure : laver immédiatement 15 min à l'eau et au savon puis consulter dans les 24 h
- Conserver le carnet de vaccination en voyage
- Rappeler que la PrEP ne dispense PAS de la PEP après une exposition
Scénario 2 : Patient consulte au retour après une morsure/griffure à l'étranger
⚠ URGENCE ABSOLUE
La rage est mortelle à ~100 % une fois symptomatique. La PEP doit être initiée sans délai.
- Anamnèse détaillée : date/lieu de la morsure, animal impliqué (espèce, comportement, vaccination connue ?), type de plaie (catégorie I/II/III), PrEP antérieure ? PEP déjà initiée sur place ?
- Soins de la plaie si non effectués : lavage eau + savon 15 min, désinfection povidone-iodée
- Si PEP non initiée ou incomplète :
- Patient non vacciné : débuter schéma complet (vaccin J0, J3, J7, J14 + RIG si catégorie III)
- Patient vacciné (≥ 2 doses PrEP) : rappel vaccinal J0, J3 (pas de RIG)
- Commander les produits : vaccin antirabique (Rabipur® ou Verorab®, disponible en pharmacie) + Bérirab® P (HRIG, stock obligatoire Suisse — contacter la pharmacie de l'hôpital cantonal si non disponible en officine)[3,4]
- Sérologie de contrôle : J14 (patient vacciné) ou J21 (patient non vacciné)[4]
- Déclaration : pas d'obligation pour l'exposition ; déclaration uniquement en cas de rage confirmée (maladie à déclaration obligatoire)[23]
- Ne pas attendre un test de l'animal pour commencer la PEP — débuter immédiatement
Scénario 3 : Morsure de chauve-souris en Suisse
- Toujours considérer comme catégorie III (morsure potentiellement invisible)[3,7]
- PEP complète (vaccin + RIG) sauf si PrEP antérieurement complétée
- Contacter le Centre suisse de la rage (Institut de virologie, Université de Berne) pour analyse de la chauve-souris si disponible[3]
Aide-mémoire — Schéma décisionnel rapide
| Situation | Action |
|---|---|
| Morsure en zone endémique, patient non vacciné, catégorie III | Lavage 15 min + vaccin J0-J3-J7-J14 + RIG J0 + sérologie J21 |
| Morsure en zone endémique, patient vacciné (≥ 2 doses PrEP) | Lavage 15 min + vaccin J0-J3 + sérologie J14 |
| Chauve-souris en Suisse, patient non vacciné | Lavage + vaccin J0-J3-J7-J14 + RIG + Centre suisse de la rage (Berne) |
| Contact catégorie I (peau intacte) | Pas de PEP |
Quand référer ?
- Exposition de catégorie III nécessitant des RIG non disponibles en officine — contacter la pharmacie hospitalière
- Patient immunodéprimé : réponse vaccinale incertaine, nécessité de suivi sérologique rapproché
- Cas complexes : PEP débutée à l'étranger de façon incomplète, schéma vaccinal non standard, grossesse
- Suspicion de rage clinique : transfert immédiat en milieu hospitalier (soins intensifs)
- Doute sur la catégorisation de l'exposition ou la conduite à tenir
Références
- WHO. Rabies vaccines: WHO position paper, April 2018. Wkly Epidemiol Rec 2018;93:201-220.
- Hampson K et al. Estimating the global burden of endemic canine rabies. PLoS Negl Trop Dis 2015;9(5):e0003786.
- OFSP/CFV. Prophylaxie pré- et postexpositionnelle de la rage humaine — Directives et recommandations. Avril 2021.
- OFSP. Mise à jour des directives et recommandations « Prophylaxie pré- et postexpositionnelle de la rage humaine ». Bull OFSP 15/2021.
- Gautret P et al. Animal-associated exposure to rabies virus among travelers, 1997-2012. Emerg Infect Dis 2015;21(4):569-577.
- Blanton JD et al. Pre-exposure rabies vaccination among US international travelers: findings from the Global TravEpiNet Consortium. PLoS Negl Trop Dis 2014;8(2):e2588.
- WHO. Protocol for a well-performed rabies post-exposure prophylaxis delivery. 2024.
- CDC Yellow Book 2026 — Rabies. Wallace RM, Shlim DR.
- Jackson AC. Demise of the Milwaukee Protocol for Rabies. Clin Infect Dis 2025;ciaf157.
- Tolentino Junior DS et al. Adapted Milwaukee protocol for rabies treatment in a Brazilian indigenous child: case report. Virology J 2024;21:265.
- Infovac.ch. Rage : la maladie et le vaccin. Mis à jour août 2025.
- Soentjens P et al. Preexposure intradermal rabies vaccination: a noninferiority trial in healthy adults on shortening the vaccination schedule from 28 to 7 days. Clin Infect Dis 2019;68(4):607-614.
- Mills DJ et al. Two-year immunogenicity of a pre-exposure rabies vaccination administered as a two-dose schedule. J Travel Med 2022;29(4):taac029.
- de Feij M et al. Delays in rabies post-exposure prophylaxis abroad. J Travel Med 2025;32(8):taaf111.
- Kessels J et al. Rabies post-exposure prophylaxis: a systematic review on abridged vaccination schedules and the effect of changing administration routes during a single course. Vaccine 2019;37(27):3533-3545.
- Murhekar MV et al. Availability of anti-rabies vaccine and rabies immunoglobulin in Indian health facilities: a nationwide cross-sectional health facility survey. Lancet Reg Health Southeast Asia 2025.
- Serum Institute of India / Lancet. Post-licensure study of Rabishield (rabies monoclonal antibody) vs ERIG in > 4000 patients. Lancet 2025.
- Ravish HS et al. Safety and tolerability of a novel monoclonal antibody cocktail for rabies post-exposure prophylaxis. npj Vaccines 2025;10:article.
- Long C et al. Developing a human monoclonal antibody combination CRM25 to prevent rabies after exposure. Int J Antimicrob Agents 2024;64(6):107383.
- SSTTM. Nouveau schéma de vaccination contre la rage pour les voyageurs. Swiss Med Forum 2018.
- Rao AK et al. Use of a modified preexposure prophylaxis vaccination schedule to prevent human rabies: recommendations of the ACIP — United States, 2022. MMWR 2022;71(18):619-627.
- OFSP. Plan de vaccination suisse 2025.
- BAG/OFSP. Rage — page d'information. Novembre 2024.