Malaria
Paludisme — Plasmodium falciparum, P. vivax, P. ovale, P. malariae, P. knowlesi
Première cause de fièvre importée chez le voyageur de retour des tropiques. En Suisse, 8 439 cas importés et 52 décès entre 1990 et 2019 (létalité ~0,6 %). L'erreur la plus fréquente du médecin de premier recours : ne pas poser la question du voyage et étiqueter le tableau comme « grippe » ou « gastro-entérite ».
Épidémiologie
Données suisses
- 1990–2019 : 8 439 cas importés, 52 décès — létalité ~0,6 %[1]
- 2013–2023 : 532 cas dont 46 cas sévères (8,6 %) ; 45/46 dus à P. falciparum
- Provenance dominante : Afrique de l'Ouest et Centrale
- Depuis 2014, P. vivax représente 36 % des cas importés (contre 11 % avant 2014), reflétant l'évolution des flux migratoires et de voyage vers l'Asie du Sud et l'Amérique latine
- P. falciparum reste l'espèce majoritaire et la seule responsable de paludisme sévère dans la cohorte suisse
Seuil suisse d'hyperparasitémie
En Suisse, le seuil de parasitémie définissant le paludisme sévère est fixé à ≥ 2 % (vs 5 % OMS, 2 % UK). Ce seuil bas est justifié par la progression rapide vers des formes sévères chez les patients non immuns au-delà de 2 %.[5]
Espèces de Plasmodium
| Espèce | Répartition | Forme clinique | Hypnozoïtes |
|---|---|---|---|
| P. falciparum | Afrique subsaharienne (prédominant), Asie du SE, Amérique du Sud | Potentiellement sévère — seule espèce causant le paludisme grave | Non |
| P. vivax | Asie du Sud, Amérique latine, Moyen-Orient, Corne de l'Afrique | Bénigne habituellement ; rechutes possibles | Oui |
| P. ovale | Afrique de l'Ouest, Asie du SE | Bénigne ; rechutes possibles | Oui |
| P. malariae | Distribution tropicale large | Bénigne ; recrudescences tardives (pas de rechutes hépatiques) | Non |
| P. knowlesi | Bornéo, Asie du SE | Zoonose simienne ; formes sévères possibles malgré parasitémie basse | Non |
Déclaration obligatoire
⚠ Déclaration obligatoire (Guide OFSP 2026)
Délai : 1 semaine pour le médecin et le laboratoire.
- Médecin → Médecin cantonal (formulaire HIN-Secure Mail, fax ou courrier postal). Critère : résultat positif d'analyses de laboratoire.
- Laboratoire → OFSP via CH-ELM (API) ou Infreport. Critère : tout résultat positif (PCR/séquençage, microscopie, mise en évidence de l'antigène). Indiquer l'espèce si connue.
⚠ Paludisme d'aéroport/de port
Des cas de paludisme transmis par des moustiques importés dans les bagages ou le fret aérien sont documentés en Suisse et en Europe, sans voyage en zone endémique. La létalité du paludisme d'aéroport/de port est élevée : 13,24 % dans une revue systématique couvrant 1969–2022, principalement en raison d'un retard diagnostique majeur.[2]
Répartition géographique
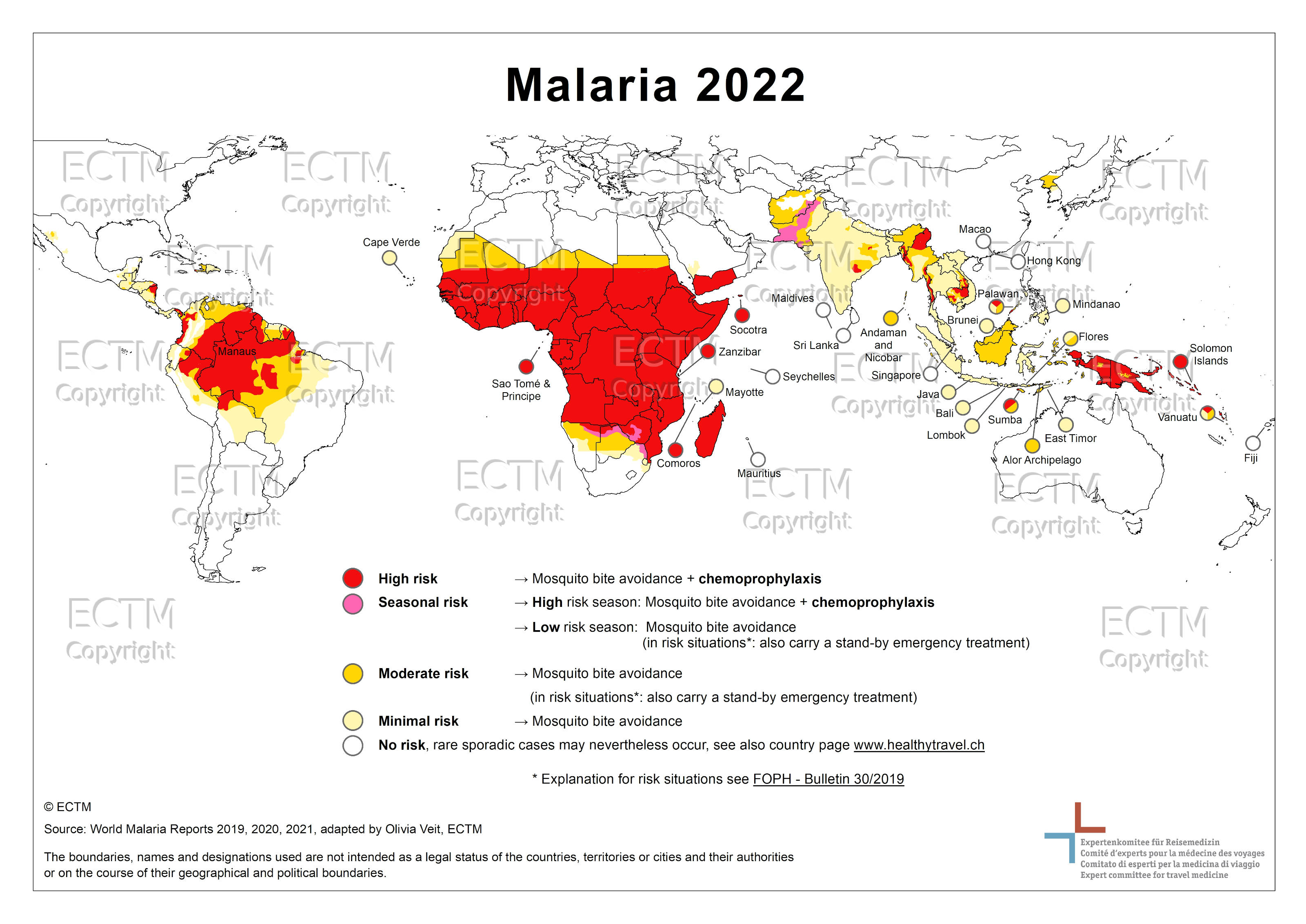
Afrique subsaharienne, Amérique centrale et du Sud, Asie du Sud et du Sud-Est, Océanie. P. falciparum prédomine en Afrique subsaharienne et P. vivax prédomine en Asie du Sud, Amérique latine et Moyen-Orient.
Transmission
- Vecteur : piqûre du moustique Anopheles femelle, piquant principalement la nuit (surtout après minuit)
- Cycle : sporozoïtes (foie) → mérozoïtes (érythrocytes) → gamétocytes (transmission au moustique)
- Hypnozoïtes : P. vivax et P. ovale forment des stades dormants dans les hépatocytes, responsables de rechutes tardives (jusqu'à 2–3 ans)
Périodes d'incubation
| Espèce | Incubation minimale | Incubation typique | Remarque |
|---|---|---|---|
| P. falciparum | 6 jours | 12–14 jours | Souvent prolongée sous prophylaxie antipaludique |
| P. vivax / P. ovale | 12 jours | ~14 jours | Rechutes possibles jusqu'à 2–3 ans (hypnozoïtes) |
| P. malariae | 18 jours | Très variable | Recrudescences tardives possibles (années) |
| P. knowlesi | 11 jours | 11–12 jours | Cycle érythrocytaire de 24 h (fièvre quotidienne) |
Clinique
Présentation initiale
Les symptômes sont souvent peu spécifiques, mimant une grippe ou une gastro-entérite : fièvre, frissons, céphalées, myalgies, fatigue, nausées, vomissements, douleurs abdominales, diarrhées, tachycardie, diaphorèse.[13]
⚠ Piège — Absence de fièvre
Jusqu'à 1/3 des patients avec paludisme ne présentent pas de fièvre lors de la consultation. Ne jamais exclure le diagnostic sur l'absence de fièvre au moment de l'examen.
Examen clinique
- Splénomégalie : fréquente, parfois volumineuse dans les infections prolongées ou récidivantes
- Ictère : modéré dans les formes non compliquées ; prononcé (bilirubine conjuguée élevée) dans les formes sévères
- Absence de rash : utile pour le diagnostic différentiel — l'absence d'exanthème oriente contre la dengue et les rickettsioses
- Formes sévères : pâleur (anémie), ictère marqué, prostration ; signes de défaillance d'organe (oligurie, confusion, détresse respiratoire)
Critères de paludisme sévère (OMS / SSTTM 2025)
| Critère | Seuil / Description |
|---|---|
| Troubles de la conscience / coma | Malaria cérébrale (Glasgow ≤ 11) |
| Anémie sévère | Hémoglobine < 7 g/dL |
| Insuffisance rénale aiguë | Créatinine > 265 µmol/L |
| SDRA | Syndrome de détresse respiratoire aiguë |
| Choc circulatoire | Hypotension réfractaire au remplissage |
| Acidose métabolique | pH < 7,25 ou lactates > 5 mmol/L |
| Ictère | Bilirubine > 50 µmol/L + autre critère de sévérité |
| Hyperparasitémie | ≥ 2 % (seuil suisse) ou ≥ 5 % (OMS)[5] |
| Hypoglycémie | < 2,2 mmol/L |
Pourquoi le seuil suisse est-il plus bas ?
Chez les patients non immuns (voyageurs, expatriés), la progression de la parasitémie au-delà de 2 % est rapide et imprévisible. Le seuil de 2 % permet une prise en charge agressive précoce, justifiant l'hospitalisation et le recours à l'artésunate IV avant l'installation d'une défaillance d'organe.[5]
Biologie
Forme non compliquée
- Thrombopénie < 150 G/L : quasi constante — valeur diagnostique élevée chez le voyageur fébrile
- Bilirubine conjuguée élevée (hémolyse + atteinte hépatique)
- Transaminases modérément élevées
- Créatinine élevée (surveillance de la fonction rénale)
- LDH élevé (marqueur d'hémolyse)
Forme sévère — critères biologiques
| Paramètre | Seuil de sévérité |
|---|---|
| Hémoglobine | < 7 g/dL |
| Glycémie | < 2,2 mmol/L |
| pH / Lactates | < 7,25 ou > 5 mmol/L |
| Créatinine | > 265 µmol/L |
| Parasitémie | ≥ 2 % (seuil suisse)[5] |
Diagnostic
| Examen | Caractéristiques | Limites |
|---|---|---|
| TDR HRP2 | Sensibilité élevée pour P. falciparum ; résultat en 15–20 min | Ne fournit pas la parasitémie ; ne détecte pas fiablement les autres espèces ; faux-négatifs par délétion hrp2/hrp3 (Afrique de l'Est, Amérique du Sud)[6] |
| Frottis + goutte épaisse | Gold standard — identification de l'espèce + quantification de la parasitémie | Préparer dans l'heure suivant le prélèvement sur EDTA ; requiert un microscopiste expérimenté |
| Répétition à 12–24 h | Si suspicion forte avec premier bilan négatif | Étude CHUV (Slack & Genton 2024, n = 4 972) : seulement 0,08 % des cas positifs détectés au 2e ou 3e test — la valeur ajoutée des tests sériés est très faible[4] |
| PCR | Référence pour confirmation d'espèce, co-infections, détection de résistance | Non disponible en urgence ; utile en cas de discordance TDR/frottis |
⚠ Piège — TDR faux-négatif et faux-positif
Un TDR négatif n'exclut pas le paludisme. Des délétions des gènes hrp2/hrp3 chez P. falciparum (Afrique de l'Est, Amérique du Sud) peuvent rendre le TDR HRP2 faussement négatif.[6] Le frottis + goutte épaisse reste indispensable. À l'inverse, un TDR peut être faussement positif dans d'autres infections fébriles du voyageur (fièvre à tique africaine notamment).[7]
En pratique : algorithme diagnostique
Devant toute fièvre au retour d'une zone endémique : TDR + frottis/goutte épaisse en urgence. Si négatif et forte suspicion clinique (thrombopénie, voyage compatible) : répéter frottis à 12–24 h. La PCR est réservée à la confirmation d'espèce ou aux discordances.[4]
Traitement
P. falciparum non compliqué
1re ligne — Artéméther-luméfantrine (Riamet®)
| Prise | Heure | Dose adulte |
|---|---|---|
| 1 | H0 | 4 comprimés |
| 2 | H8 | 4 comprimés |
| 3 | H24 | 4 comprimés |
| 4 | H36 | 4 comprimés |
| 5 | H48 | 4 comprimés |
| 6 | H60 | 4 comprimés |
- Prendre avec un repas gras (améliore l'absorption de la luméfantrine)
- ECG non systématique aux doses standard recommandées : la luméfantrine peut allonger le QTc mais sans effet arythmogène cliniquement significatif aux doses thérapeutiques
- ECG indiqué si : QT long congénital, arythmie symptomatique, cardiopathie sévère, co-prescription de médicaments allongeant le QTc (quinine, quinidine, antipsychotiques, antidépresseurs), inhibiteurs puissants du CYP3A4 (kétoconazole), ou traitement antérieur par halofantrine (contre-indiqué dans le mois suivant l'artéméther-luméfantrine)
- Note : le paludisme lui-même peut modifier le QTc — toute anomalie ECG n'est pas imputable au médicament
⚠ Piège — Patient > 65 kg sous Riamet
L'efficacité du Riamet est de 100 % chez les patients ≤ 65 kg mais seulement 90,4 % chez les patients > 65 kg.[3] Taux d'échec tardif de 5,2 % à J20–J28 chez les voyageurs non immuns européens.[3b] Planifier systématiquement un frottis de contrôle à J28. Considérer Malarone comme alternative chez les patients > 65 kg ou en retour du Grand Mékong.
Alternative — Atovaquone-proguanil (Malarone®)
- 4 comprimés/j × 3 jours (adulte), avec repas gras
- Option préférentielle en retour du Grand Mékong (résistances artémisinine) ou patient > 65 kg[12]
P. falciparum sévère — Artésunate IV
| Moment | Dose | Voie |
|---|---|---|
| H0 | 2,4 mg/kg | IV |
| H12 | 2,4 mg/kg | IV |
| H24 | 2,4 mg/kg | IV |
| Puis toutes les 24 h | 2,4 mg/kg | IV |
- Relais oral (Riamet ou Malarone) dès que parasitémie ≤ 1 %
- Hospitalisation obligatoire
⚠ PADH — Hémolyse différée post-artésunate
Survient chez 15–22 % des voyageurs traités par artésunate IV (certaines séries rapportent jusqu'à 27 %).[8] Délai : J7–J30 post-traitement.
Mécanisme : « pitting » splénique des érythrocytes parasités avec libération différée de l'hémoglobine résiduelle.
Surveillance obligatoire : Hb + LDH + haptoglobine 1×/semaine pendant 4 semaines après arrêt de l'artésunate IV.[9,10]
P. vivax / P. ovale — Prévention des rechutes
Traiter l'accès aigu (chloroquine si souche sensible ; ACT si résistance chloroquine). Puis traitement radical des hypnozoïtes hépatiques :
| Médicament | Posologie | Prérequis | Remarques |
|---|---|---|---|
| Primaquine | 0,25–0,5 mg/kg/j × 14 jours (adulte : 15–30 mg/j) |
Test G6PD OBLIGATOIRE — risque d'hémolyse sévère | Si G6PD déficient : régime hebdomadaire sous supervision |
| Tafénoquine | 300 mg dose unique | G6PD ≥ 70 % de la normale | Avantage : dose unique (meilleure observance). Risque : hémolyse prolongée si G6PD déficient (demi-vie longue, hémolyse impossible à stopper). Contre-indiquée en grossesse.[11] |
⚠ Test G6PD obligatoire
Ne jamais prescrire primaquine ou tafénoquine sans résultat de G6PD. L'hémolyse peut être fatale chez les patients déficients. La tafénoquine est particulièrement dangereuse car sa demi-vie longue rend l'hémolyse impossible à arrêter une fois déclenchée.[11]
P. malariae / P. knowlesi
- P. malariae : sensible à la chloroquine dans la plupart des régions ; pas d'hypnozoïtes (pas de rechute hépatique)
- P. knowlesi (Bornéo, Asie du Sud-Est) : parasite simien ; peut provoquer des formes sévères malgré une parasitémie apparemment faible (érythrocytes non élargis). Traiter comme P. falciparum sévère en cas de doute clinique.
Prévention
Mesures anti-vectorielles
- Moustiquaire imprégnée d'insecticide (dormir sous moustiquaire en zone endémique)
- Répulsifs cutanés à base de DEET (20–50 %) ou d'icaridine
- Vêtements longs et de couleur claire, imprégnés de perméthrine
- Rappeler que l'Anopheles pique principalement la nuit
Chimioprophylaxie
| Médicament | Posologie adulte | Début | Fin après retour | Remarques |
|---|---|---|---|---|
| Atovaquone-proguanil (Malarone®) | 1 cp/j | J-1 | 7 jours | Bien toléré ; courte durée post-exposition ; option de choix pour séjours courts |
| Doxycycline | 100 mg/j | J-1 | 28 jours | Économique ; photosensibilité, troubles digestifs ; contre-indiquée < 8 ans et grossesse |
| Méfloquine (Lariam®) | 250 mg/sem | 2–3 sem avant | 4 semaines | Effets neuropsychiatriques possibles ; intérêt pour séjours longs ; contre-indiquée si ATCD psychiatriques |
Rappel pour le praticien
La chimioprophylaxie ne garantit pas une protection à 100 %. Des cas de paludisme sous prophylaxie correctement prise existent. L'incubation est souvent prolongée en cas de prophylaxie, rendant le diagnostic encore plus tardif. Toute fièvre au retour d'une zone endémique doit faire évoquer le paludisme, même sous prophylaxie.
Pièges & perles
⚠ Piège 1 — Ne pas poser la question du voyage
L'erreur la plus fréquente et la plus grave du médecin de premier recours : ne pas demander l'anamnèse de voyage devant un tableau fébrile non spécifique. Le diagnostic de « grippe » ou « gastro-entérite » est souvent posé à tort. Tout patient fébrile devrait être interrogé sur un séjour en zone tropicale dans les 3 mois précédents.
⚠ Piège 2 — TDR négatif = paludisme exclu ?
Non. Le TDR HRP2 peut être faussement négatif (délétions hrp2/hrp3) ou faussement positif (rickettsiose, fièvre typhoïde).[7] Le frottis + goutte épaisse reste indispensable. Si premier bilan négatif avec forte suspicion clinique : répéter à 12–24 h.[4]
⚠ Piège 3 — Patient > 65 kg sous Riamet
Taux d'échec tardif d'environ 10 % (recrudescence J15–J29) chez les patients > 65 kg.[3] Planifier systématiquement un frottis de contrôle à J28. Considérer Malarone si poids > 65 kg ou retour du Grand Mékong.
⚠ Piège 4 — PADH méconnu
L'anémie hémolytique J7–J30 après artésunate IV est souvent diagnostiquée à tort comme une rechute parasitaire. Ne pas omettre la surveillance Hb + LDH + haptoglobine pendant 4 semaines post-traitement.[8]
✦ Perles cliniques
- Thrombopénie : quasi constante dans le paludisme — sa présence chez un voyageur fébrile a une forte valeur d'orientation diagnostique
- Suivi J28 obligatoire pour tout patient > 65 kg traité par Riamet : frottis de contrôle pour exclure une recrudescence tardive
- Surveillance PADH après artésunate IV : Hb + LDH + haptoglobine 1×/semaine pendant 4 semaines
- G6PD : toujours doser avant primaquine ou tafénoquine — l'hémolyse peut être fatale
Conduite pratique
Au cabinet — Suspicion de paludisme
- Anamnèse de voyage : destination, dates, prophylaxie antipaludique prise/non prise, observance
- Bilan urgent : TDR + frottis/goutte épaisse, FSC, créatinine, bilirubine, transaminases, LDH, glycémie, CRP
- Si TDR ou frottis positif : identifier l'espèce, quantifier la parasitémie, rechercher les critères de sévérité
- Si négatif avec forte suspicion : répéter frottis à 12–24 h ; ne pas laisser rentrer le patient sans suivi planifié
- Déclaration obligatoire dans la semaine
Algorithme de traitement simplifié
| Situation | Traitement | Suivi |
|---|---|---|
| P. falciparum non compliqué, ≤ 65 kg | Riamet® 6 prises / 3 jours | Frottis J3, J7 |
| P. falciparum non compliqué, > 65 kg | Riamet® ou Malarone® | Frottis J3, J7, J28 |
| P. falciparum sévère ou parasitémie ≥ 2 % | Artésunate IV → relais oral | Frottis /12–24h ; PADH 4 sem |
| P. vivax / P. ovale | Chloroquine ou ACT + primaquine/tafénoquine | G6PD obligatoire avant 8-aminoquinoléines |
| P. malariae | Chloroquine | Contrôle standard |
| P. knowlesi (doute clinique) | Traiter comme P. falciparum | Frottis sériés |
Quand référer
Référer sans délai dans les situations suivantes :
- Tout critère de paludisme sévère (altération de conscience, détresse respiratoire, insuffisance rénale, choc, acidose)
- Hyperparasitémie ≥ 2 % (seuil suisse)
- Suspicion de P. knowlesi
- Échec thérapeutique (recrudescence sous traitement bien conduit)
- Grossesse
- Enfant en bas âge avec fièvre au retour des tropiques
- Doute diagnostique persistant (TDR/frottis discordants, espèce non identifiée)
✦ Consultation spécialisée
Pour toute question ou cas complexe, un avis spécialisé peut être obtenu via traveldoctor.ch/professionnels.
Références
- Giannone B et al. Imported malaria in Switzerland (1990–2019): A retrospective analysis. Travel Med Infect Dis 2022;45:102233. DOI:10.1016/j.tmaid.2022.102233
- Balzli D et al. Airport/seaport and autochthonous malaria in Europe from 1969 to 2022: A systematic review. New Microbes New Infect 2025;67:101627. DOI:10.1016/j.nmni.2025.101627
- Vuuren C van et al. Weight-based treatment failure risk with artemether-lumefantrine in non-immune travelers. J Travel Med 2024.
- Sonden K et al. High rate of treatment failures in nonimmune travelers treated with artemether-lumefantrine for uncomplicated P. falciparum malaria in Sweden: retrospective study. Clin Infect Dis 2017;64:199–207.
- Slack A, Genton B. Usefulness of serial testing for the diagnosis of malaria. J Travel Med 2024;31:taae030.
- SSTTM. Malaria Treatment Recommendations 2025.
- Maltha J, Jacobs J. Clinical practice: the diagnosis of imported malaria in children. Eur J Pediatr 2011;170:821–829. DOI:10.1007/s00431-011-1451-4
- Zewude RT et al. False-positive malaria rapid diagnostic test likely due to African tick bite fever in a returning traveler. Reports (MDPI) 2024;7(4):100. DOI:10.3390/reports7040100
- Jaureguiberry S et al. Delayed-onset hemolytic anemia in patients with severe malaria treated with artesunate, France, 2011–2013. Emerg Infect Dis 2015;21:804–812.
- Travis J et al. Treatment failure and post-artesunate delayed haemolysis in a returned traveller from Uganda with partially drug-resistant severe P. falciparum malaria. Med J Aust 2026;224:e70136. DOI:10.5694/mja2.70136
- Murphy F et al. From 64% hyperparasitemia to recovery: Managing severe falciparum malaria and delayed hemolytic anemia. IJID Reg 2025;15:100644. DOI:10.1016/j.ijregi.2025.100644
- Hanboonkunupakarn B, White NJ. Advances and roadblocks in the treatment of malaria. Br J Clin Pharmacol 2020;88:374–382. DOI:10.1111/bcp.14474
- Visser MT et al. Are national treatment guidelines for falciparum malaria in line with WHO recommendations? Trop Med Int Health 2022;27:129–136. DOI:10.1111/tmi.13715
- Thwaites GE, Day NP. Approach to fever in the returning traveler. N Engl J Med 2017;376:548–560.