Fièvre jaune
Yellow fever — Flavivirus, famille des Flaviviridae
Arbovirose à haute mortalité transmise par Aedes aegypti, endémique en Afrique et en Amérique du Sud. La vaccination (Stamaril) reste la pierre angulaire de la prévention. Résurgence alarmante en 2025 dans les Amériques. Aucun traitement antiviral spécifique approuvé.
Épidémiologie
Charge mondiale
- L'OMS estime 67 000–173 000 infections sévères et 31 000–82 000 décès par an en Afrique et dans les Amériques[1]
- Incidence environ 10x plus élevée en Afrique qu'en Amérique du Sud[2]
- 45 pays endémiques : 34 en Afrique, 11 en Amérique centrale/du Sud[1]
- Aucun cas jamais rapporté en Asie malgré la présence d'Aedes aegypti — raisons non entièrement comprises (immunité croisée dengue ? facteurs génétiques du vecteur ?)
Situation 2023–2025
Amériques (OMS/OPS)
- 2023 : 41 cas confirmés, 23 décès (CFR ~56 %) dans 4 pays[3]
- 2024 : 61 cas confirmés, 30 décès (CFR ~49 %) dans 5 pays[3]
- 2025 (au 26 avril) : 212 cas confirmés, 85 décès (CFR 40 %) dans 5 pays — triplement par rapport à 2024 ; cas détectés hors bassin amazonien (São Paulo, Tolima/Colombie)[3]
- Mai 2025 (OPS) : augmentation ×8 des cas par rapport à la même période en 2024 ; risque public élevé en raison de cas proches de zones urbaines densément peuplées[4]
- Octobre 2025 (OPS/COP30) : 294 cas confirmés, 121 décès dans 6 pays (ajout de la Guyane) ; 1 cas importé au Costa Rica[5]
⚠ Alerte 2025
Quasiment tous les cas 2024–2025 dans les Amériques sont survenus chez des individus non vaccinés. La couverture vaccinale post-COVID est insuffisante : 10/12 pays endémiques sous les seuils cibles.[4]
Afrique (OMS AFRO)
- Depuis début 2023 : 13 pays de la région AFRO ont rapporté des cas probables/confirmés (RDC, Nigeria, Cameroun, Burkina Faso, Côte d'Ivoire, etc.)[6]
- CFR préliminaire 2023 en Afrique : ~11 %[6]
- Stratégie EYE (Eliminate Yellow Fever Epidemics) de l'OMS : campagnes de vaccination de masse en cours[7]
Contexte suisse
- Maladie à déclaration obligatoire (OFSP/BAG) — délai 1 semaine[8]
- Cas importés extrêmement rares : un seul cas diagnostiqué en Suisse ces dernières années chez un voyageur de retour[8]
- Aucun risque de transmission autochtone (pas d'Aedes aegypti en Suisse)
- Vaccination disponible uniquement dans les centres de vaccination agréés (liste sur healthytravel.ch) ou chez un médecin accrédité
- Capacité diagnostique européenne pour la fièvre jaune : besoin de renforcement selon une évaluation externe de 36 laboratoires[35]
Répartition géographique
Afrique
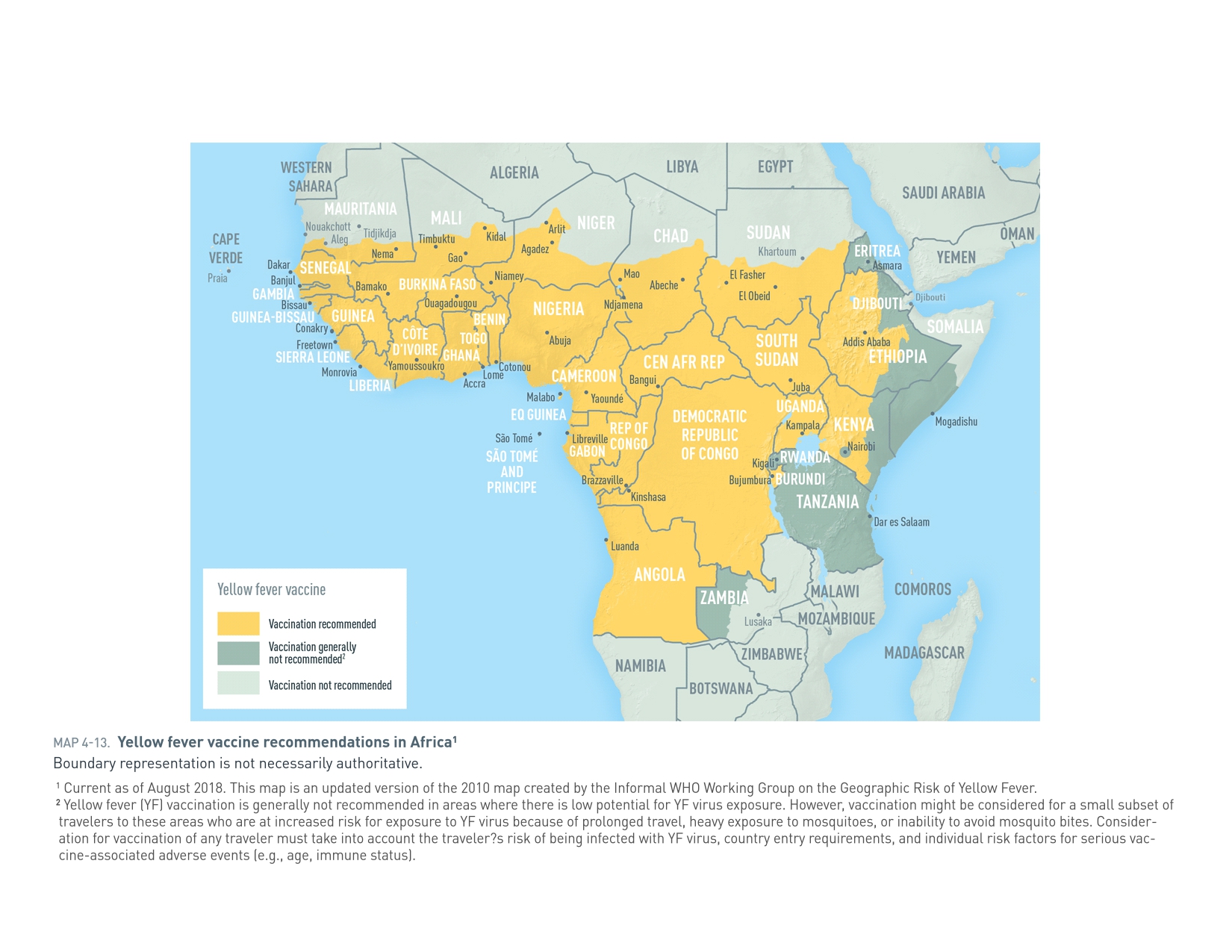
Amériques
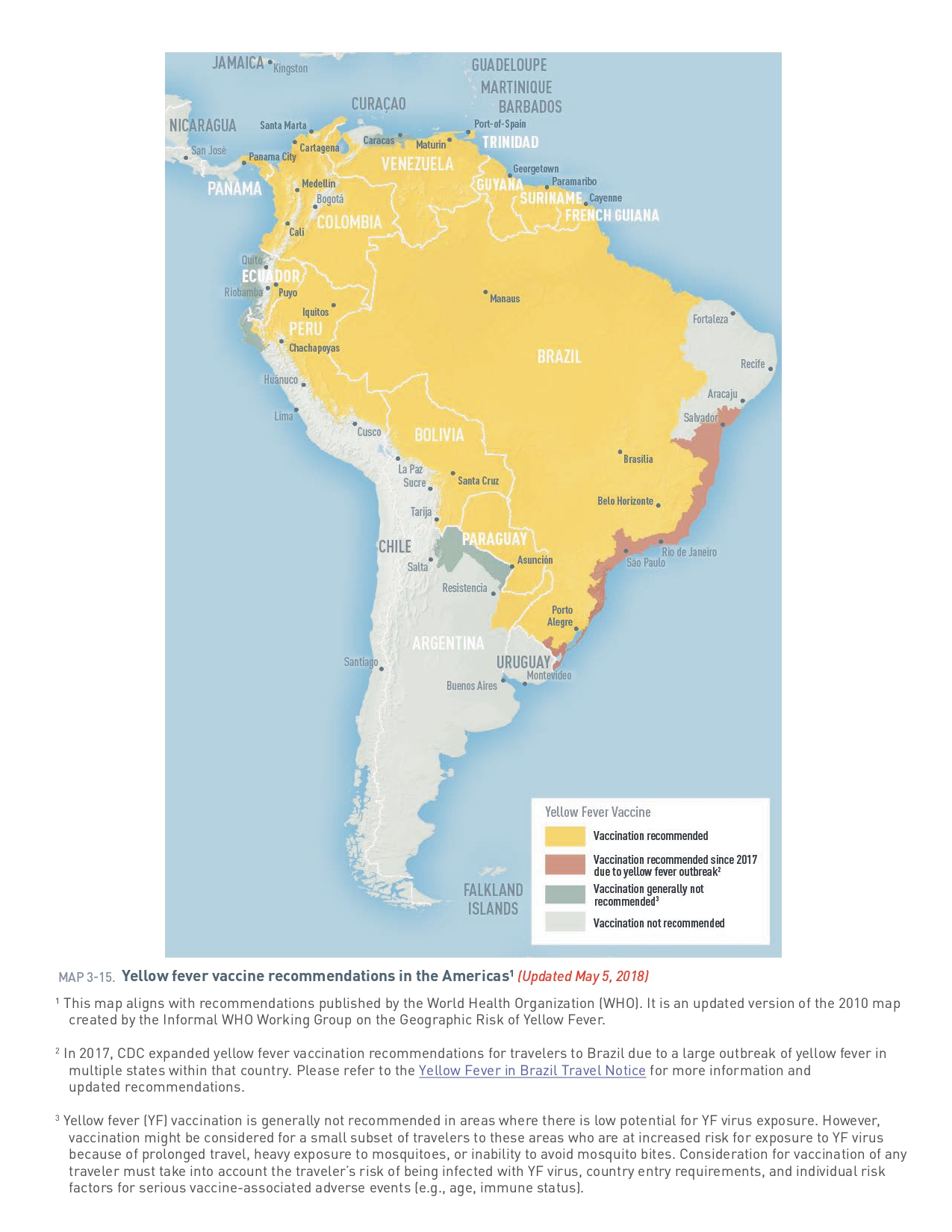
Transmission
- Agent causal : virus de la fièvre jaune, Flavivirus à ARN, famille des Flaviviridae (apparenté à dengue, zika, encéphalite japonaise, West Nile, encéphalite à tiques)
- Vecteur principal : Aedes aegypti (cycle urbain) ; Haemagogus et Sabethes (cycle sylvatique, Amériques) ; Aedes africanus (cycle sylvatique, Afrique)
- Piqûre diurne (principalement en fin de journée)
- Trois cycles épidémiologiques : sylvatique (primates non humains ↔ moustiques sylvatiques), intermédiaire/savane (humains ↔ moustiques semi-domestiques), urbain (humain ↔ Ae. aegypti)
- Incubation : 3–6 jours (maximum 10 jours)[9]
Présentation clinique
Évolution classique en trois phases. La majorité des infections sont paucisymptomatiques ou asymptomatiques. Parmi les patients symptomatiques, 15–25 % évoluent vers la phase toxique.[9]
Phase 1 — Infection (J1–J3)
- Fièvre élevée d'apparition subite, frissons, céphalées, myalgies (surtout dorso-lombaires)
- Nausées, vomissements
- Signe de Faget : bradycardie relative malgré la fièvre (dissociation pouls-température) — très évocateur
- La majorité des patients guérissent à ce stade
Phase 2 — Rémission (J3–J4)
- Amélioration transitoire de quelques heures à 48h
- Piège diagnostique : le patient peut être renvoyé à domicile
Phase 3 — Intoxication (J4–J7+)
- Ictère (d'où le nom « fièvre jaune »)
- Insuffisance hépatique : ASAT > ALAT (atteinte médio-zonale typique = corps de Councilman), PAL discrètement élevée[10]
- Coagulopathie : déficit de synthèse des facteurs vitamine K-dépendants + coagulopathie consomptive (D-dimères élevés survenant indépendamment de la destruction hépatocytaire)[36]
- Diathèse hémorragique : hématémèse (« vomito negro »), méléna, épistaxis, saignements gingivaux, ecchymoses
- Insuffisance rénale aiguë avec protéinurie importante
- Troubles neurologiques : agitation, convulsions, délire, coma
- Choc circulatoire
⚠ Mortalité de la phase toxique : 20–50 %
Jusqu'à 50–60 % dans certaines séries. L'évolution vers la défaillance multiorganique est rapide une fois la phase toxique installée.[9,10]
Particularité histopathologique
- Nécrose hépatocytaire médio-zonale (zone 2 du lobule) — très évocatrice de fièvre jaune (contrairement aux hépatites virales qui touchent la zone périportale)[10]
- Corps de Councilman : corps apoptotiques éosinophiles (pathognomoniques mais non spécifiques)
- Détection virale immunohistochimique dans le foie, les reins, la rate, le coeur et les poumons[37]
Biologie
| Paramètre | Anomalie typique |
|---|---|
| Formule sanguine | Leucopénie (parfois thrombopénie) |
| ASAT / ALAT | Très élevées, ASAT > ALAT (atteinte hépatique + musculaire) |
| Phosphatases alcalines | Discrètement élevées |
| Bilirubine | Élevée (ictère) |
| TP / INR | TP diminué, INR augmenté (coagulopathie) |
| D-dimères | Élevés (coagulopathie consomptive)[36] |
| Créatinine / urée | Élevées (IRA) |
| Protéinurie | Importante |
| Lactate | Élevé si choc |
Diagnostic
Phase aiguë (J1–J5 post-symptômes)
- RT-PCR : détection du génome viral dans le sérum — test de choix en phase virémique (J1–J5). Après J5, la virémie chute et la PCR devient moins sensible[11]
- Isolement viral : possible mais réservé aux laboratoires de référence (BSL-3)
Phase tardive (à partir de J5–J7)
- Sérologie IgM (ELISA) : positive à partir de J5–J7 ; attention aux réactions croisées avec d'autres Flavivirus (dengue, zika, West Nile, encéphalite japonaise, encéphalite à tiques) et avec la vaccination antiflavivirus antérieure[12,13]
- Sérologie IgG : séroconversion ou augmentation ≥ 4× du titre en sérum pairé (aigu + convalescent à 14–21 jours d'intervalle)
- PRNT (Plaque Reduction Neutralization Test) : test de confirmation le plus spécifique, mais réactivité croisée possible si co-infections/vaccinations multiples contre des Flavivirus[12]
Laboratoire de référence en Suisse
CRIVE (Centre national de référence pour les infections virales émergentes), HUG Genève : RT-PCR et sérologie de confirmation disponibles[14]
Algorithme diagnostique pratique
- Suspicion clinique (fièvre + ictère + voyage en zone endémique) → bilan hépatique + coagulation + formule sanguine + fonction rénale
- J1–J5 : envoyer sérum pour RT-PCR au CRIVE
- À partir de J5 : sérologie IgM/IgG (paire) — attention réactivité croisée
- Confirmation : PRNT avec panel de Flavivirus
- Déclaration obligatoire dès que cas confirmé ou suspect
Diagnostic différentiel
| Diagnostic | Éléments distinctifs |
|---|---|
| Paludisme | Frottis/goutte épaisse + TDR ; pas d'ictère précoce typique ; coinfection possible |
| Dengue sévère | Hémoconcentration, thrombopénie profonde, fuite plasmatique ; sérologie croisée possible |
| Hépatites virales (A, B, E) | ALAT > ASAT ; pas de diathèse hémorragique précoce |
| Leptospirose | Ictère + IRA + myalgies ; suffusion conjonctivale ; sérologie/PCR spécifique |
| Fièvres hémorragiques virales (Ebola, Marburg, Lassa) | Contexte épidémiologique ; mesures d'isolement d'emblée ; PCR spécifique |
| Fièvre typhoïde | Fièvre en plateau, tuphos, splénomégalie, leucopénie ; hémocultures |
| Rickettsiose | Escarre d'inoculation ; rash ; sérologie |
⚠ Point clé
La fièvre jaune doit être évoquée chez tout voyageur fébrile avec ictère de retour d'une zone endémique, vacciné ou non (échecs vaccinaux décrits, rares).[40]
Traitement
Pas de traitement antiviral spécifique approuvé
- Prise en charge de support : réhydratation, correction des troubles électrolytiques, transfusion si nécessaire, dialyse en cas d'IRA, support en soins intensifs
- Cristalloïdes plutôt que colloïdes pour la réanimation liquidienne IV[38]
- Guidage de la réanimation par le temps de recoloration capillaire et le lactate[38]
⚠ Médicaments à éviter
- AINS : l'OMS (2025) recommande formellement contre l'usage des AINS dans toute arbovirose aiguë — risque d'aggravation hémorragique[38]
- Aspirine : même contre-indication (risque hémorragique accru)
- Paracétamol à doses élevées : hépatotoxicité sur foie déjà lésé. L'OMS suggère néanmoins le paracétamol pour la douleur et la fièvre dans les formes non sévères[38]
Consensus colombien — fièvre jaune sévère (2025)
Premier consensus formel sur la prise en charge des patients critiques : monitoring hépatique serré, correction de la coagulopathie, support rénal, prise en charge du choc (Forero-Delgadillo et al. Lancet Reg Health Am 2025).[39]
Piste thérapeutique émergente : sofosbuvir
- Inhibiteur de la polymérase NS5B, approuvé pour l'hépatite C ; activité in vitro et in vivo contre le virus de la fièvre jaune[15]
- Cohorte Brésil 2018 (n = 21) : diminution progressive de la charge virale sous sofosbuvir 400 mg/j ; nécessité d'essais randomisés[16]
- Cas rapporté 2025 : utilisation comme prophylaxie post-exposition après administration inadvertante du vaccin chez un patient à risque de YEL-AVD — évolution favorable[17]
- Statut : hors AMM, pas d'essai randomisé achevé ; à considérer dans un contexte compassionnel
Prévention — Vaccination
Vaccin Stamaril
- Stamaril (Sanofi Pasteur) : vaccin vivant atténué, souche 17D-204, cultivé sur oeufs de poule embryonnés SPF
- Voie d'administration : sous-cutanée (SC)
- Dose : 0,5 mL (≥ 1000 UI)
- Délai de validité : le certificat international est valide 10 jours après la vaccination
- Le vaccin 17D est considéré comme l'un des vaccins vivants les plus efficaces jamais développés (introduction en 1937)[40]
Schéma vaccinal
| Situation | Schéma |
|---|---|
| Primovaccination | 1 dose unique → protection à vie (OMS, depuis 2013) |
| RSI (Règlement sanitaire international) | Certificat valide à vie depuis le 11 juillet 2016 (amendement annexe 7 du RSI)[18] |
| Rappel (position suisse ECTM/SSTTM) | Un rappel est recommandé après 10 ans si voyage à haut risque (séjour prolongé en zone de haute endémicité ou d'épidémie)[30] |
| Rappel CDC/ACIP (USA) | Rappel considéré pour : voyageurs en zone d'épidémie, femmes enceintes au moment de la 1re dose, PVVIH, greffe de cellules souches[19] |
Débat sur la durée de protection
- Arguments pour une protection à vie : anticorps neutralisants détectables chez >80 % des vaccinés après 20–35 ans ; mémoire immunitaire cellulaire T persistante[20,21]
- Arguments pour un rappel : déclin d'anticorps chez certains sous-groupes (enfants vaccinés <2 ans, PVVIH, femmes enceintes)[22] ; bénéfice immunologique de la revaccination démontré (Ferrara et al. J Travel Med 2025)[23]
- Échecs vaccinaux : rares mais documentés sur 8 décennies, surtout chez des patients immunodéprimés ou vaccinés dans la petite enfance[40]
Position pragmatique suisse (ECTM/SSTTM)
Rappel recommandé après 10 ans en cas de voyage à haut risque — approche plus prudente que l'OMS, justifiée par l'évidence d'un déclin chez certains sous-groupes et par le profil non-immun des voyageurs suisses.[30]
Contre-indications absolues
| Contre-indication | Détail |
|---|---|
| Âge < 6 mois | Risque accru d'encéphalite post-vaccinale |
| Allergie sévère aux oeufs | Anaphylaxie confirmée aux protéines d'oeuf |
| Allergie au vaccin ou composant | Réaction anaphylactique antérieure au Stamaril |
| Immunodéficience sévère | VIH avec CD4 < 200/mm3 ou < 15 % (enfant < 6 ans) ; immunosuppresseurs ; chimiothérapie ; greffe d'organe[24] |
| Pathologie du thymus | Thymome, thymectomie (risque majeur de YEL-AVD)[24] |
Précautions (vaccination après évaluation bénéfice/risque)
| Précaution | Conduite |
|---|---|
| Âge ≥ 60 ans (primovaccination) | Risque accru de YEL-AVD et YEL-AND ; vacciner uniquement si risque réel d'exposition significatif[24,25] |
| Âge 6–8 mois | Évaluation au cas par cas |
| VIH asymptomatique, CD4 200–499/mm3 | Séroprotection réduite (~61 %) ; rappel recommandé ; vérifier titres[26] |
| Grossesse | Risque théorique pour le foetus ; reporter si possible ; si voyage inévitable en zone d'épidémie : vaccination possible |
| Allaitement | Cas rapportés de transmission vaccinale au nourrisson via le lait maternel → prudence si nourrisson < 6 mois |
| Immunosuppression temporaire | Reporter la vaccination d'au moins 4 semaines après arrêt des corticoïdes systémiques (≥ 14 jours de traitement) ou de l'immunosuppresseur |
| Allergie légère aux oeufs | Vaccination possible en milieu hospitalier avec surveillance |
Interactions avec d'autres vaccins vivants
Si non administrés simultanément, respecter un intervalle minimum de 4 semaines entre deux vaccins vivants (ROR, varicelle, Qdenga, etc.).
Effets indésirables graves — YEL-AND et YEL-AVD
YEL-AND (Yellow Fever Vaccine-Associated Neurotropic Disease)
- Incidence : 0,25–0,8 pour 100 000 doses[24,27]
- Délai : 3–28 jours post-vaccination
- Présentations : méningo-encéphalite, syndrome de Guillain-Barré, ADEM, paralysie de nerfs crâniens
- Série française (Le Hir et al. 2024) : virémie vaccinale prolongée et réponse auto-immune chez certains patients ; majorité avec évolution favorable[28]
- Mortalité : < 5 % ; pronostic généralement favorable
YEL-AVD (Yellow Fever Vaccine-Associated Viscerotropic Disease)
- Incidence globale : 0,3–0,4 pour 100 000 doses[24]
- Chez les ≥ 60 ans : 1,0–1,8 pour 100 000 doses ; chez les ≥ 70 ans : 3,2 pour 100 000 doses[24,25]
- Délai : 2–5 jours post-vaccination
- Tableau clinique : maladie multisystémique mimant la fièvre jaune sauvage — fièvre, ictère, insuffisance hépatique, coagulopathie, défaillance multiorganique
- Mortalité : ~43–65 %[24]
| Facteur de risque de YEL-AVD | Détail |
|---|---|
| Âge ≥ 60 ans | Primovaccination ; risque multiplié par 3–10 vs adultes jeunes[42] |
| Pathologie du thymus | Thymome ou thymectomie (17 % des premiers cas rapportés)[24] |
| Immunodéficience non reconnue | Surtout primovaccination |
⚠ Message clé pour le médecin de premier recours
Avant toute primovaccination fièvre jaune chez un patient ≥ 60 ans ou avec antécédent thymique, évaluer soigneusement le rapport bénéfice/risque. Si le risque d'exposition est faible (transit aéroportuaire, séjour urbain court dans un pays avec exigence réglementaire mais faible risque réel), préférer un certificat d'exemption médicale plutôt que la vaccination.
Sécurité vaccinale chez les immunodéprimés
Méta-analyse systématique (Wigg de Araujo Lagos et al. J Travel Med 2023) : RR d'effets indésirables chez les immunodéprimés vs non-immunodéprimés = 1,00 (IC 95 % 0,78–1,29). Pas de surrisque clairement démontré, mais données limitées pour les immunodéficiences sévères.[41]
Doses fractionnées
- En cas de pénurie vaccinale lors d'épidémies, l'OMS recommande l'utilisation de doses fractionnées (1/5 de la dose standard) depuis 2016[29]
- Séroconversion après dose fractionnée : > 85 % à 28 jours ; protection d'au moins 12 mois démontrée[29,31]
- Immunogénicité comparable à la dose standard à court terme ; données de durée à long terme encore insuffisantes[45]
- Le certificat RSI délivré après dose fractionnée est valide 1 an (et non à vie)
- Utilisé avec succès lors des épidémies de Kinshasa (RDC) 2016, São Paulo (Brésil) 2018
Pièges & perles cliniques
Fièvre jaune méconnue chez le voyageur fébrile
Maladie rare chez le voyageur vacciné mais pas impossible (échecs vaccinaux décrits).[40] Doit être évoquée devant toute fièvre + ictère au retour d'une zone endémique. Le diagnostic différentiel avec la dengue sévère et les hépatites virales est critique.
Réactions croisées sérologiques avec d'autres Flavivirus
Un patient précédemment vacciné contre la fièvre jaune, l'encéphalite japonaise, l'encéphalite à tiques, ou ayant eu une dengue, peut présenter des IgM/IgG croisées rendant le diagnostic sérologique difficile. Solution : PRNT avec panel de Flavivirus ; RT-PCR en phase aiguë.
Primovaccination chez le sujet âgé (≥ 60 ans)
Risque de YEL-AVD multiplié par 3–10 par rapport aux adultes jeunes. Le MG doit poser la question du thymus (thymome, thymectomie) avant toute vaccination. Si doute ou patient immunofragile : adresser à un centre de médecine des voyages.
Certificat à vie ≠ immunité à vie
Le RSI accepte le certificat à vie, mais cela ne signifie pas que l'immunité est éternelle chez tous les patients. PVVIH, enfants vaccinés < 2 ans, femmes enceintes lors de la vaccination : immunité potentiellement insuffisante → vérifier titres et/ou revacciner.
AINS formellement contre-indiqués
L'OMS recommande formellement contre l'usage des AINS dans toute arbovirose aiguë, quel que soit le degré de sévérité.[38] Risque d'aggravation hémorragique.
Perles
- La bradycardie relative (signe de Faget) chez un voyageur fébrile et ictérique est très évocatrice de fièvre jaune
- ASAT > ALAT dans le contexte d'une hépatite fébrile post-voyage : penser fièvre jaune (nécrose médio-zonale + rhabdomyolyse)
- La coagulopathie de la fièvre jaune sévère est en partie consomptive (D-dimères élevés), pas uniquement un déficit de synthèse hépatique[36]
- Sofosbuvir 400 mg/j = piste thérapeutique émergente en cas de YEL-AVD ou de fièvre jaune sévère (utilisation compassionnelle, hors AMM)[16,17]
- En 2025, quasiment tous les cas rapportés aux Amériques sont survenus chez des non-vaccinés — argument fort pour la vaccination pré-voyage[4]
Conduite pratique pour le médecin de premier recours
Pré-voyage (conseil vaccinal)
- Vérifier si la destination nécessite la vaccination (exigence RSI et/ou risque réel d'exposition)
- Vérifier le statut vaccinal antérieur et la date de la dernière dose
- Si primovaccination ≥ 60 ans ou pathologie du thymus : évaluer le rapport bénéfice/risque ; envisager un certificat d'exemption si risque d'exposition faible
- Si immunodépression (VIH, immunosuppresseurs, greffe) : adresser à un centre de médecine des voyages
- Rappeler que le certificat est valide 10 jours après la vaccination — anticiper
- Si rappel recommandé (position suisse ECTM/SSTTM) : après 10 ans pour voyage à haut risque
Post-voyage (suspicion clinique)
- Suspicion clinique : fièvre + ictère au retour d'une zone endémique (même si vacciné)
- Bilan initial : NFS, bilan hépatique complet (ASAT, ALAT, PAL, bilirubine), coagulation (TP, INR, D-dimères), créatinine, urée, bandelette urinaire (protéinurie), lactate
- Exclure le paludisme en parallèle : frottis/goutte épaisse + TDR
- J1–J5 : envoyer sérum pour RT-PCR fièvre jaune au CRIVE (HUG Genève)
- ≥ J5 : sérologie IgM/IgG (paire) ; confirmation par PRNT
- Déclaration obligatoire dès la suspicion
- Si forme sévère : hospitalisation en soins intensifs sans délai
Quand référer ?
- Suspicion de fièvre jaune : tout voyageur fébrile avec ictère de retour d'une zone endémique
- Conseil vaccinal complexe : patient ≥ 60 ans, immunodéprimé, pathologie du thymus, femme enceinte/allaitante
- Effet indésirable vaccinal suspect : symptômes neurologiques ou viscérotropes dans les 28 jours post-vaccination
- Forme sévère : phase toxique avec ictère, hémorragies, défaillance d'organe → soins intensifs en urgence
Références
- WHO. Yellow fever fact sheet. 2024. who.int
- CDC Yellow Book 2026. Yellow Fever. Staples JE, O'Laughlin K. cdc.gov
- WHO. Disease Outbreak News: Yellow fever — Region of the Americas. May 2025. who.int
- PAHO. Public health risk of yellow fever remains high in the Americas. Rapid Risk Assessment, 27 May 2025. paho.org
- PAHO. COP30 in Belém: PAHO recommends yellow fever and measles vaccination for travelers. October 2025. paho.org
- WHO AFRO. Epidemiological Situation of Yellow Fever in Africa, 2024–2025. who.int [PDF]
- WHO. Eliminate Yellow Fever Epidemics (EYE) Strategy. who.int
- OFSP/BAG. Fièvre jaune — Maladies et agents pathogènes. bag.admin.ch
- Monath TP, Vasconcelos PFC. Yellow fever. J Clin Virol. 2015;64:160–173.
- Quaresma JA et al. Midzonal lesions in yellow fever: a specific pattern of liver injury caused by direct virus action and in situ inflammatory response. Med Hypotheses. 2006;67(3):618–621. DOI
- WHO. Yellow fever: detection and laboratory diagnosis. 2018. who.int [PDF]
- Maeda A, Maeda J. Review of diagnostic plaque reduction neutralization tests for flavivirus infection. Vet J. 2013;195(1):33–40.
- Oliveira RA et al. Serological cross-reactivity among common flaviviruses. Front Cell Infect Microbiol. 2022;12:975398. DOI
- CRIVE — Centre national de référence pour les infections virales émergentes, HUG Genève. hug.ch
- de Freitas CS et al. Yellow fever virus is susceptible to sofosbuvir both in vitro and in patients with acute liver failure. PLoS Negl Trop Dis. 2019;13(10):e0007072. DOI
- Mendes EA et al. Sofosbuvir off-label treatment of yellow fever patients during an outbreak in Brazil, 2018: a cohort study. Open Forum Infect Dis. 2024;11(6):ofae312. DOI
- Barrett J et al. Sofosbuvir as post-exposure prophylaxis for yellow fever-associated viscerotropic disease (YEL-AVD). J Antimicrob Chemother. 2025;80(3):825–827. DOI
- WHO. Amendment to International Health Regulations (2005), Annex 7 (yellow fever). 2016. who.int [PDF]
- CDC/ACIP. Yellow Fever Vaccine Booster Doses: Recommendations. MMWR 2015;64(23):647–650. cdc.gov
- Amanna IJ, Slifka MK. Questions regarding the safety and duration of immunity following live yellow fever vaccination. Expert Rev Vaccines. 2016;15(12):1519–1533. DOI
- Hombach J et al. Review of data and knowledge gaps regarding yellow fever vaccine-induced immunity and duration of protection. npj Vaccines. 2020;5:54. DOI
- Long-term immunity following yellow fever vaccination: a systematic review and meta-analysis. Lancet Infect Dis. 2025. nitag-resource.org
- Ferrara et al. Is a second dose of yellow fever vaccine needed? A systematic review of humoral and cell-mediated immunity after revaccination. J Travel Med. 2025;32(8):taaf106. DOI
- Porudominsky R, Gotuzzo EH. Yellow fever vaccine and risk of developing serious adverse events: a systematic review. BMC Infect Dis. 2018;18(1):241. DOI
- Seligman SJ. Risk groups for yellow fever vaccine-associated viscerotropic disease (YEL-AVD). Vaccine. 2014;32(44):5769–5775. DOI
- WHO Global Advisory Committee on Vaccine Safety. Yellow fever vaccine and HIV infection. who.int
- Lecomte E et al. A clinician's perspective on yellow fever vaccine-associated neurotropic disease. J Travel Med. 2020;27(7):taaa172. DOI
- Le Hir A, Durand GA, Boucraut J et al. Yellow fever vaccine-associated neurologic and viscerotropic disease: a 10-year case series. J Travel Med. 2024;31(2):taad160. DOI
- WHO. Fractional doses of the yellow fever vaccine. Q&A, 2017. who.int
- Bühler S, Jaeger VK, Kling K, Hatz C. To vaccinate or let it be — current recommendations and the reality about yellow fever vaccination. Swiss Med Wkly. 2014;144:w14095. DOI
- Martins RM et al. Immune response induced by standard and fractional doses of 17DD yellow fever vaccine. npj Vaccines. 2024;9:50. DOI
- UK Medicines and Healthcare products Regulatory Agency. Stamaril SmPC. medicines.org.uk
- UK Green Book Chapter 35: Yellow fever. March 2024. travelhealthpro.org.uk [PDF]
- WHO. Urban Yellow Fever Risk Management: Draft Handbook. October 2025. who.int [PDF]
- Presser LD et al. Excellent capability for molecular detection of Aedes-borne dengue, Zika, and chikungunya viruses but with a need for increased capacity for yellow fever and Japanese encephalitis viruses. J Clin Microbiol. 2024;62(12):e00910-24. DOI
- Bailey AL et al. Consumptive coagulopathy of severe yellow fever occurs independently of hepatocellular tropism and massive hepatic injury. Proc Natl Acad Sci USA. 2020;117(51):32648–32656. DOI
- Ferreira MS et al. Experimental yellow fever virus infection in the squirrel monkey. Mem Inst Oswaldo Cruz. 2020;115:e190501. DOI
- WHO. Guidelines for clinical management of arboviral diseases: dengue, chikungunya, Zika and yellow fever. Geneva: WHO; 2025. ISBN 978-92-4-011111-0. who.int
- Forero-Delgadillo JM et al. Colombian consensus on the care of critically ill patients with suspected or confirmed severe yellow fever. Lancet Reg Health Am. 2025;52:101144. DOI
- Coulter MC et al. Breakthroughs and insights: A comprehensive review of yellow fever vaccine breakthrough infection across 8 decades. Vaccine. 2024;42(25):126423. DOI
- Wigg de Araujo Lagos B et al. Yellow fever vaccine safety in immunocompromised individuals: a systematic review and meta-analysis. J Travel Med. 2023;30(1):taac095. DOI
- de Abreu FVS et al. A systematic review and a meta-analysis of the yellow fever vaccine in the elderly population. Vaccines (Basel). 2022;10(5):711. DOI
- McClenathan BM et al. Incidence of anaphylaxis to YF-VAX yellow fever vaccination: a retrospective evaluation. J Travel Med. 2024;31(1):taad154. DOI
- Farnsworth A et al. Real-world evidence of yellow fever vaccination data-driven study. Vaccine. 2025;43(4):126758. DOI
- Nnaji CA et al. Immunogenicity and safety of fractional dose yellow fever vaccination: A systematic review and meta-analysis. Vaccine. 2020;38(9):2282–2290. DOI